Les arythmies cardiaques représentent un défi clinique, économique et sociétal. Avec le vieillissement des populations, l’augmentation des comorbidités (hypertension, obésité, diabète) et les progrès du diagnostic, leur prévalence ne fait qu’augmenter (la fréquence peut dépasser 10% chez les plus de 80 ans). Selon une étude publiée dans The Lancet en 2024, le nombre de personnes vivant avec la fibrillation auriculaire (FA) dans le monde est passé de 33,5 millions à 59 millions entre 2010 et 2019. La FA multiplie par 5 le risque d’accident vasculaire cérébral et par 3 le risque d’insuffisance cardiaque. De même, les malades d’arythmie cardiaque présentent une mortalité accrue de 40 à 50% par rapport aux personnes saines. En Europe, des études récentes montrent que le fardeau de la FA et de la flutter auriculaire est en croissance depuis le début des années 1990, tant en termes de prévalence (+67% du nombre de cas entre 1990 et 2021) que de mortalité (+120% sur la même période) et d’années de vie ajustées sur l’invalidité (+80%). Cette étude montre par ailleurs que les facteurs de risque précédemment cités gagnent du terrain dans les populations les plus jeunes ce qui doit être perçu comme un enjeu important des politiques de santé pour les années à venir.
Dans ce contexte, les méthodes de traitement classiques sont remises en question, notamment en termes de coût, d’accessibilité et d’impact environnemental. L’innovation, et particulièrement la miniaturisation, offre une voie prometteuse. Cette note propose un état des lieux des traitements classiques des arythmies, afin d’en présenter les limites face aux défis sociétaux. Seront également abordées les tendances de miniaturisation en cardiologie et dispositifs implantables, qu’une exploration du positionnement d’Olva Medical, start-up médicale accompagnée par Unitec dans ce paysage en pleine évolution.
Unitec x Les Echos Judiciaires Girondins
Retrouvez « La veille techno » : la note de veille Unitec version courte qui met en avant une start-up accompagnée ! Ce mois-ci, notre #PépiteUnitec Olva Medical est à l’honneur.
Qu’est-ce qu’une arythmie ?
Le cœur, qui ne dépend pas uniquement des muscles, est une pompe électrique : chaque battement est déclenché par un signal électrique émis par le nœud sinusal, situé dans l’oreillette droite, qui se propage dans ses cavités. Ce signal est normalement émis de manière régulière et déclenche la contraction des cavités cardiaques dans le bon ordre, assurant une circulation efficace du sang dans le corps. Quand ce signal est perturbé, le rythme devient trop rapide, trop lent ou irrégulier : c’est l’arythmie. La plus fréquente, la fibrillation auriculaire, touche des millions de personnes en Europe et augmente fortement le risque d’accident vasculaire cérébral (AVC). Les symptômes – palpitations, essoufflement, fatigue – peuvent être bénins mais parfois graves, nécessitant une prise en charge rapide. Avec le vieillissement de la population, les arythmies deviennent un enjeu de santé publique majeur.
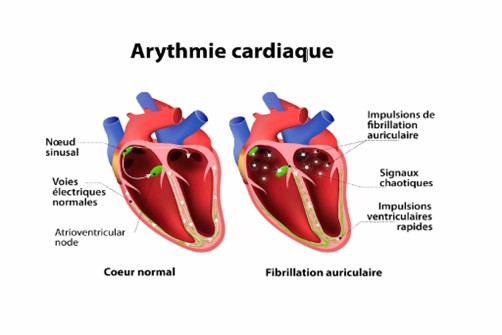
Les grandes formes d’arythmie
L’arythmie est donc un dysfonctionnement du rythme cardiaque. Elle peut prendre plusieurs formes.
- La tachycardie : le rythme cardiaque est trop rapide. Par exemple, dans certaines formes, le cœur peut battre à plus de 150–200 battements par minute (bpm), même au repos.
- La bradycardie : le rythme est trop lent. Le cœur peut battre à moins de 50 battements par minute, ce qui peut entraîner fatigue, étourdissements, voire des syncopes si le débit sanguin devient insuffisant.
- La fibrillation auriculaire (FA) : c’est la forme la plus fréquente d’arythmie. Dans la FA, les oreillettes ne se contractent pas de façon coordonnée ; elles “tremblent” (elles fibrillent) de façon chaotique, à des fréquences très élevées (jusqu’à 400–600 impulsions par minute) dans les oreillettes. Cela entraine une conduction irrégulière vers les ventricules, provoquant un rythme cardiaque irrégulier et souvent rapide.
- La flutter auriculaire : dans ce cas, les oreillettes battent beaucoup trop vite (environ 250 à 300 battements par minute) mais contrairement à la FA, les battements sont réguliers. L’influx électrique tourne en boucle dans l’oreillette droite créant un circuit automatique mais régulier qui ne transmet qu’une impulsion sur deux, trois voire quatre. La conduction vers les ventricules est régulière mais peut entrainer des palpitations rapides et régulières, des vertiges. La flutter peut favoriser la formation de caillots sanguins dans les oreillettes entrainant un risque accru d’AVC mais également favoriser la tachycardie (affaiblissement du muscle cardiaque).
- Tachycardie ventriculaire : ici l’origine du dérèglement est dans les ventricules. Cette forme est plus grave car elle peut se transformer en fibrillation ventriculaire, un état dans lequel le cœur cesse de pomper efficacement — situation d’urgence pouvant conduire à un arrêt cardiaque.
Les traitements classiques des arythmies
Si toutes les arythmies ne sont pas malignes (certaines s’arrêtent d’elles-mêmes ou par un changement de comportement comme l’arrêt du tabac ou un changement de régime alimentaire), d’autres sont dangereuses ou suffisamment gênantes pour nécessiter un traitement qu’il soit chimique, mécanique ou électronique.
Médicaments anti-arythmies et de contrôle de la fréquence
Les médicaments restent la première ligne de traitement pour beaucoup de patients. Ils stabilisent l’activité électrique ou ralentissent le cœur :
- Contrôle du rythme : l’idée est de tenter de ramener le cœur à un rythme normal (dit sinusal) par l’administration de médicaments comme l’amiodarone, le flécaïnide ou le sotalol.
- Contrôle de la fréquence : ralentir la vitesse des battements ventriculaires pour améliorer la tolérance de l’arythmie, sans forcément supprimer la fibrillation auriculaire. On trouve dans cette catégorie de médicaments les bêta-bloquants ou les inhibiteurs calciques.
Le principal avantage de la médicamentation chimique est qu’il s’agit de traitements simples (même s’il est souvent nécessaire de combiner plusieurs molécules pour atteindre un résultat positif) et largement disponible et accessible. Cependant, ces médicaments ne sont pas la solution miracle et présentent également quelques limites : une efficacité inconstante et des risques d’effets secondaires qui peuvent être lourds (troubles thyroïdiens ou pulmonaires avec l’amiodarone, pro-arythmie possible avec certains médicaments).
La cardioversion
La cardioversion est une procédure médicale utilisée lorsque l’arythmie est récente ou mal tolérée et elle consiste à ramener un rythme sinusal régulier du cœur par différentes méthodes :
- Par décharge électrique : un choc électrique externe, administré sous courte anesthésie, “réinitialise” le cœur et le ramène en rythme normal.
- Par la pharmacologique : qui consiste en l’injection intraveineuse d’antiarythmiques (ex. flécaïnide, amiodarone) pour stopper l’arythmie.
L’utilisation de cette procédure permet un rétablissement rapide du rythme sinusal mais augmente le risque de récidive. Par ailleurs, avant d’entamer toute cardioversion, le praticien doit s’assurer de l’absence de caillot dans l’oreillette pour éviter tout risque d’AVC.
L’ablation par cathéter
L’ablation par cathéter est aujourd’hui la technique de référence pour beaucoup d’arythmies, en particulier la fibrillation auriculaire, le flutter et certaines tachycardies.
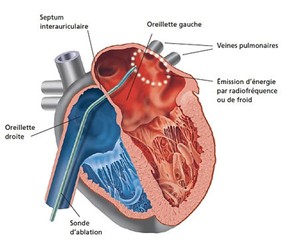
Le chirurgien cardiaque introduit un ou plusieurs cathéters en passant par des veines (le plus souvent la veine fémorale) jusqu’au cœur. Ces sondes enregistrent directement l’activité électrique et détectent la zone en cause. Une fois celle-ci identifiée, une source d’énergie est propulsée pour détruire ou isoler la zone responsable. Il existe plusieurs techniques comme la radiofréquence qui utilise la chaleur, la cryothérapie (qui utilise le froid), le laser ou les ultrasons.
Les dispositifs implantables
Les arythmies peuvent également être traitées par l’implantation d’un dispositif permanent qui permet de réguler les battements du cœur ou de prévenir tout risque d’arrêt brutal.
On retrouve les stimulateurs cardiaques (pacemakers) qui sont des petits dispositifs généralement implantés sous la peau et reliés au cœur par des sondes et qui envoie des impulsions électriques lorsque le rythme est trop lent. Ces batteries ont des durées de vie assez longues (entre 7 et 10 ans), sont fiables et sont indiquées dans le cas de bradycardies notamment. Le défibrillateur automatique implantable (DAI) est un appareil implanté qui surveille de manière continue le rythme cardiaque du patient. En cas de tachycardie ventriculaire ou de fibrillation, un choc électrique est envoyé pour réguler le rythme cardiaque. Ce procédé est particulièrement indiqué pour les personnes sujettes à crise cardiaque.
Les pacemakers et défibrillateurs implantables font partie des dispositifs les plus fiables de toute la médecine moderne, avec des taux de survie très élevés à long terme.
La chirurgie cardiaque
Dans les cas les plus complexes, la chirurgie cardiaque est utilisée. On trouve les interventions lourdes comme les pontages, le remplacement valvulaire (TAVI) mais aussi d’autres procédures comme Maze qui consiste à réaliser de petites incisions ou des cautérisations dans les oreillettes pour créer des cicatrices qui bloquent les circuits électriques anormaux et permet de traiter la fibrillation auriculaire. En technique ouverte, le patient est relié à une machine cœur poumon artificielle ce qui en fait une technique particulièrement lourde.
Les limites des approches classiques
Si les traitements contre l’arythmie permettent de sauver de nombreuses vies et d’offrir aux malades la possibilité de vivre normalement, il n’en reste pas moins que ces traitements et interventions présentent également un certains nombres de limites et de faiblesses.
Premièrement, tous les traitements ont un coût particulièrement élevé et une infrastructure lourde. A titre d’exemple, les procédures d’électrophysiologie nécessitent des équipements coûteux : une salle d’ablation complète (système de cartographie 3D, générateur, cathéters, monitoring) qui peut coûter jusqu’à 1 million d’euros. Chaque ablation peut coûter, selon les techniques et les pays, entre 7000 et 15000 euros. Seules les grandes structures hospitalières disposent de ces équipements (en France 70 centres hospitaliers pratiquent ces ablations et sont situés dans les grandes métropoles) et certains pays en développement n’ont pas les moyens financiers de pratiquer ces ablations obérant les chances de survie des malades (selon le WHO Global Health Report 2022, moins de 10% des patients éligibles à une ablation peuvent en bénéficier).
Deuxièmement, la complexité technique des interventions reste élevée avec notamment un risque de complications non négligeable. Les chirurgiens doivent naviguer à l’intérieur des cavités cardiaques avec une précision millimétrique et si elles restent exceptionnelles (1% à 3% des cas), les complications existent : perforation de la paroi du cœur, atteinte de l’œsophage, thrombose, embolie ou infection post-opératoire. Les personnes âgées, cardiaques, diabétiques ou obèses sont encore plus exposées à ces risques.
Si l’ablation est très efficace, elle n’est pas infaillible. De nombreuses études médicales (EP Europace, ScienceDirect, Cardiovascular Prevention and Pharmacotherapy) mettent en exergue le fait que très souvent (entre 20% et 50% des cas) les patients opérés ont connu une récidive d’arythmie après opération nécessitant une deuxième intervention. Une étude publiée en 2023 dans la revue EU Europace montre que 1400 patients sur un échantillon de 4250 présentaient une récidive clinique à 5 ans (notamment due à une reconnexion des veines pulmonaires), suggérant ainsi la possibilité que la fibrillation auriculaire pourrait être une maladie chronique évolutive.
Un impact écologique sous-estimé
Le secteur de la santé représente plus de 4% des émissions mondiales de gaz à effet de serre, ce qui ferait de ce secteur l’équivalent du 5ème pays en terme d’émission de CO². Une étude chinoise publiée en juin 2025 montre que dans les hôpitaux de Shangai, la mjeure partie de l’empreinte provient de la production, du transport, de l’usage et de l’élimination des dispositfis médicaux ainsi que la consommation d’énergie, des gaz anesthésiques, etc…
Mais le vrai défi reste la gestion des déchets et des dispositifs à usage unique. En électrophysiologie, comme dans beaucoup d’interventions cardiaques, on utilise de nombreux dispositifs à usage unique stériles (cathéters, sondes, isolants, champs stériles, électrodes, seringues, etc.). Une grande partie de ces éléments ne peut pas être récupérée ou recyclée en raison des contraintes de stérilité, des matériaux composites ou des réglementations de sécurité. Un étude publiée dans la revue EP Europace en février 2023 estime que le poids total des émissions de CO2 équivalentes liées à une ablation s’élève en moyenne à 77kg CO-eq par procédure. Une autre étude a quantifié que dans un centre cardiaque, on générait chaque année environ 11 tonnes de déchets recyclables et près de 30 tonnes de déchets contaminés rien que pour les procédures invasives et de cathétérisme (nom donné aux interventions médicales qui permettent d’explorer les structures du cœur). Lorsqu’on extrapole à l’échelle mondiale des laboratoires de cathétérisme et salles opératoires cardiaques, cela représenterait jusqu’à 150 150 000 tonnes de déchets annuels. Cette explosion de la production de déchets est la conséquence du développement du jetable et du dispositif à usage unique. Pour concilier haute technologie et écologie, l’une des pistes prometteuses est le reconditionnement et la réutilisation de dispositifs initialement conçus pour un usage unique. Dans des scénarios optimisés, on peut envisager des réductions d’émissions de jusqu’à 60 % par dispositif reconditionné. Toutefois, ce réemploi doit surmonter des défis majeurs : préserver les propriétés physiques des dispositifs après stérilisation, éviter la contamination, garantir la conformité réglementaire. Des études ont documenté des micro-défauts après plusieurs cycles de reconditionnement tandis que d’autres recherches montrent que dans certains cas (comme pour des scalpels chirurgicaux), les versions réutilisables peuvent avoir une empreinte carbone jusqu’à 8,6 fois inférieure à celle de leurs homologues jetables, même en tenant compte de la stérilisation.
La révolution de la miniaturisation
La miniaturisation est l’une des tendances les plus marquantes de la médecine moderne. Elle consiste à rendre les dispositifs médicaux plus petits, plus précis et plus intelligents, grâce à l’intégration de capteurs, de composants électroniques à faible consommation et parfois de capacités de connectivité. Dans le domaine de la cardiologie interventionnelle et de l’électrophysiologie, cette tendance transforme profondément la manière de diagnostiquer et de traiter les troubles du rythme cardiaque. A titre d’exemple, Medtronic commercialise un stimulateur cardiaque révolutionnaire, Micra, implanté directement dans le cœur à l’aide d’une technique minimalement invasive et qui ne nécessite pas l’utilisation de sondes. Mesurant à peine 2 centimètres et pesant 2 grammes, il a une durée de vie de 17 ans et ses risques d’infection sont réduits d’environ 25% par rapport aux autres modèles.

Les progrès ne concernent pas que les pacemakers. Dans les salles d’électrophysiologie, là où l’on traite les arythmies, les équipements prenaient autrefois toute la place : ordinateurs géants, écrans, câbles, capteurs. Aujourd’hui, grâce à la miniaturisation, les cardiologues utilisent des cathéters ultrafins et des logiciels de cartographie 3D capables de repérer une anomalie électrique du cœur avec une précision millimétrique. Ces outils permettent de traiter le problème sans ouvrir la poitrine, souvent en moins de deux heures, et avec un simple point de ponction à la jambe. Autre exemple. Abbott propose des systèmes de cartographie 3D pour cœur, notamment le EnSite X EP System, couplé à des cathéters de haute densité. Ces dispositifs permettent de créer une carte électro-anatomique du cœur en 3D, très précise et en quasi-temps réel. Grâce à ces technologies, les cardiologues peuvent localiser exactement la zone à traiter, ce qui améliore la précision de l’ablation. La cartographie 3D haute densité et la navigation précise rendent les interventions plus sûres, plus efficaces, et potentiellement plus rapides — des atouts essentiels pour la miniaturisation “logistique” (moins de matériel encombrant, moins d’exposition aux rayons X, etc.). Ces innovations permettent d’intervenir de façon moins invasive, de réduire la durée d’hospitalisation, d’alléger les coûts, et même d’ouvrir la voie à une médecine plus durable. Elles traduisent une évolution majeure : passer de systèmes hospitaliers lourds à des dispositifs portables, autonomes et parfois réutilisables.
Olva Medical : réinventer l’électrophysiologie durable
Le modèle actuel basé sur les ablations par cathéter est devenu économiquement et écologiquement intenable :
- Chaque intervention mobilise du matériel très coûteux : environ 1,5 million d’euros en équipements (systèmes de cartographie, générateurs, amplificateurs, fluoroscopie).
- Les consommables à usage unique (cathéters, câbles, sondes) coûtent en moyenne 7000 € par intervention, alors que le financement perçu par les hôpitaux publics est de l’ordre de 3500 € par intervention.
Résultat : ces procédures sont structurellement déficitaires pour les hôpitaux. À cela s’ajoute un problème environnemental majeur : la dépendance à des dispositifs jetables, responsables d’une empreinte carbone élevée et d’une production massive de déchets médicaux non recyclables.
Face à cette situation, Olva Medical, jeune startup accompagnée par Unitec propose une réinvention complète de l’électrophysiologie. Sa solution repose sur un système portable, réutilisable et modulaire qui intègre :
- une baie d’électrophysiologie dans un format compact,
- des cathéters réutilisables.
Des impacts environnementaux considérables
Olva Medical vise une réduction moyenne de 85 % des émissions de gaz à effet de serre par rapport aux cathéters jetables. Ses estimations reposent sur une analyse de cycle de vie intégrant :
- la fabrication (1,75 kg CO₂-eq/cathéter neuf) ;
- les méthodes de stérilisation (0,15 à 0,6 kg CO₂-eq/cycle)
En atteignant 20 cycles de réutilisation, la réduction d’impact serait autour de 80 %.
Outre la réduction des déchets, la solution d’Olva permet de rapatrier la chaîne de valeur en Europe – conception, production, stérilisation et maintenance locales – contribuant ainsi à la souveraineté industrielle et à la création d’emplois qualifiés en ingénierie, qualité et logistique.
INTERVIEW / 3 questions à : Guillemette Duchateau, CEO et co-fondatrice Olva Medical
Que proposez-vous ?
Notre plateforme contribue à réduire de manière significative le coût des équipements et des consommables nécessaires aux procédures d’ablation par cathéter. Ces interventions restent très onéreuses : environ 1,5 M€ d’équipements par salle et près de 5 000 € de consommables par intervention, principalement en raison de l’utilisation de cathéters à usage unique. Pour lever ces freins, nous développons une plateforme interventionnelle portable et compacte, déployable dans des environnements moins spécialisés. Elle permettra à un plus grand nombre d’établissements de santé de proposer ces traitements.
Quels sont les avantages majeurs de cette solution ?
Nos cathéters sont conçus pour être réutilisables dès l’origine : réduction du coût, diminution des risques de pénurie de matériel, et amélioration de l’empreinte environnementale à la clé.
Les cathéters à usage unique sont très polluants : ce sont des dispositifs médicaux complexes, contenant de l’électronique et des métaux rares, produits via une chaîne mondialisée, et utilisés de quelques minutes à plusieurs heures. Un gaspillage de ressources considérable que nous souhaitons diminuer en développant des cathéters réutilisables des dizaines de fois.
Comment Unitec contribue-t-il au développement de votre technologie ?
Unitec nous aide à naviguer dans un secteur très complexe, avec des spécificités fortes. Les dispositifs médicaux suivent un parcours clinique et réglementaire long, de plusieurs années, avant d’accéder au marché. Il est impératif de mobiliser beaucoup de financement avant même la commercialisation, et donc essentiel de savoir activer les bons financements, publics et privés. C’est aussi une aventure qui demande de coordonner des acteurs publics et privés très différents : hôpitaux, centres de recherche, financeurs et partenaires. Un acteur comme Unitec, avec un chargé d’affaires spécialisé santé qui connaît bien le secteur et ses acteurs, est un accélérateur majeur.






